Química quântica explora as origens da energia
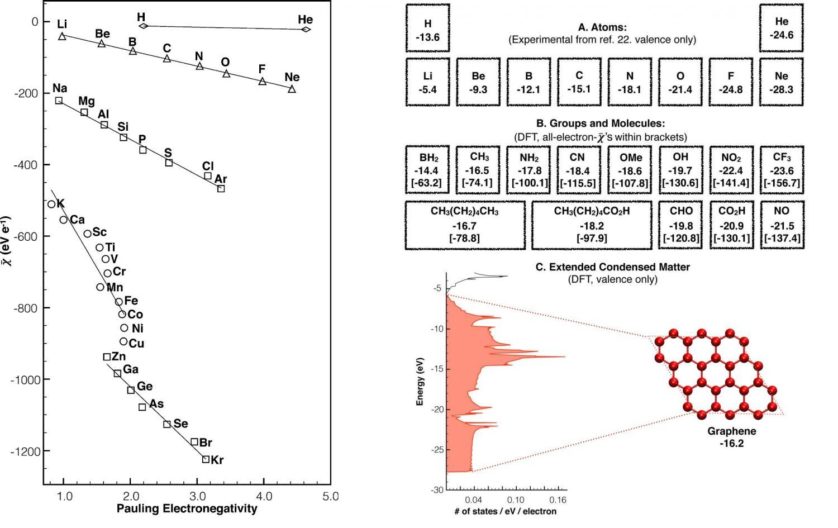
A definição alternativa de eletronegatividade proposta por Allen produz valores experimentais que se correlacionam de forma linear com valores determinados pela definição tradicional de Pauling. A imagem mostra valores calculados de eletronegatividade para átomos e moléculas selecionados
Depois de mostrarmos a palavra “quântica” tantas vezes no Hype ao lado das palavras “física” e “mecânica”, chegou a vez da química quântica. Em um novo estudo, pesquisadores adentraram esse mundo do minúsculo nas reações químicas, procurando desvendar os mistérios da energia.
Origens da energia em reações químicas
Todas as reações químicas têm uma coisa em comum: envolvem algum tipo de mudança na energia. Em grande escala, essa mudança geralmente pode ser medida de várias formas para fins práticos, mas a tentativa de compreender as origens fundamentais desta energia em escalas cada vez menores é mais complicada, especialmente conforme a química entra no domínio do quântico.
Em um novo estudo publicado no Journal of the American Chemical Society, os químicos Martin Rahm e Roald Hoffmann, da Universidade de Cornell (EUA), exploraram uma nova forma de compreender as origens da energia em reações químicas no nível quântico.
O artigo foca na ideia amplamente aceita de que todas as interações entre moléculas, átomos e elétrons que ligam átomos podem coletivamente ser entendidas em termos de energia. No entanto, as origens desta energia, e como ela muda durante uma reação química, permanecem questões em aberto.
Decomposição de energia
Rahm e Hoffmann propuseram um novo tipo de análise de decomposição de energia. Eles afirmam que o total de mudança de energia ocorrida em qualquer reação química pode ser dividido em três componentes: repulsão nuclear-nuclear (a energia repulsiva entre os núcleos carregados positivamente de átomos diferentes), a energia média de elétrons ligados (a energia média necessária para remover um elétron de um átomo), e a interação elétron-elétron (a energia repulsiva entre elétrons carregados negativamente).
Os cientistas explicam em seu artigo o que acontece quando quaisquer dois átomos são aproximados.
Em primeiro lugar, a repulsão entre os dois núcleos aumenta, o que faz com que os elétrons se movam entre os núcleos numa tentativa de se proteger desta repulsão. Na presença dos dois núcleos, a energia média dos elétrons ligados muda devido a diferenças na atração de elétrons nucleares. À medida que os elétrons se aproximam, eles também começam a interagir mais fortemente um com o outro. A quantificação destas interações elétron-elétron é um dos maiores desafios na química computacional.
Eletronegatividade
Em seu artigo, os químicos sugerem novas possibilidades de compreensão da energia usando uma interpretação alternativa de um dos conceitos mais fundamentais da química, o de eletronegatividade.
A eletronegatividade foi tradicionalmente definida por Linus Pauling em 1932 como “o poder de um átomo de atrair elétrons para si mesmo”. Essa é a definição mais utilizada até hoje.
Uma definição alternativa, proposta em 1989 por Lee Allen, é que a eletronegatividade é a energia de ligação média de elétrons de valência (Rahm e Hoffmann usam todos os elétrons, e não apenas os de valência, na sua proposta). Valores de eletronegatividade obtidos usando a definição de Allen correlacionam fortemente com os obtidos usando a de Pauling, mas a principal vantagem da definição de Allen é que a eletronegatividade definida desta maneira pode ser medida experimentalmente (por exemplo, usando espectroscopia de fotoelétron), enquanto a eletronegatividade utilizando a definição de Pauling não pode ser medida.
A capacidade de medir experimentalmente a energia média de elétrons ligados, juntamente com o fato de os dados experimentais poderem ser usados para determinar a repulsão nuclear-nuclear e interações elétron-elétron, fornece algumas habilidades sem precedentes. Mais importante ainda, torna-se possível medir experimentalmente a percentagem de variação de energia total pela qual cada um dos três componentes é responsável.
Oito classes de reação
Com esta informação, os cientistas explicam que todas as reações químicas e transformações físicas podem ser classificadas em oito tipos, com base em se a reação consome ou libera energia e o fato de ser favorecida ou resistida pelos componentes. Isso pode fornecer informações valiosas sobre a natureza de uma ligação química.
Os químicos também demonstraram que, em quatro das oito classes de reações, o conhecimento apenas da energia de ligação é suficiente para prever ou não se a reação é susceptível de continuar.
Este artigo é o primeiro de uma série na qual os pesquisadores planejam aprofundar estas ideias, especialmente no que diz respeito à utilidade potencial desta nova perspectiva de energia em reações químicas.
Aplicações
Uma perspectiva “tentadora” é a possibilidade de medir energias absolutas, enquanto a maioria da química refere-se à medida de energias relativas. Um experimento começaria com a energia absoluta medida conhecida de um sistema de um elétron (por exemplo, C5+, que é um átomo de carbono com todos menos um dos seus elétrons removidos), que pode ser facilmente medido uma vez que, com apenas um elétron, existe zero repulsão elétron-elétron.
Em seguida, a energia absoluta do átomo de carbono, e as interações elétron-elétron no seu interior, podem ser medidas conforme elétrons são adicionados, um a um. Este feito deve ser possível, uma vez que é em princípio possível medir experimentalmente a energia média dos elétrons ligados de cada etapa.
“Este artigo tem três resultados importantes”, disse Rahm. “Ele conecta o conceito químico central da eletronegatividade com o total de energia, cujas alterações governam a maioria da química. Ele nos diz como podemos estimar a importância das interações elétron-elétron no governo das reações químicas, a partir de dados experimentais. É também o primeiro esquema de decomposição de energia que pode ser aplicado indistintamente usando dados computados ou experimentais ou ambos, o que deve permitir pontes interdisciplinares”.
No futuro, os cientistas pretendem aplicar esta compreensão teórica para estudar uma variedade de reações químicas. [Phys]

