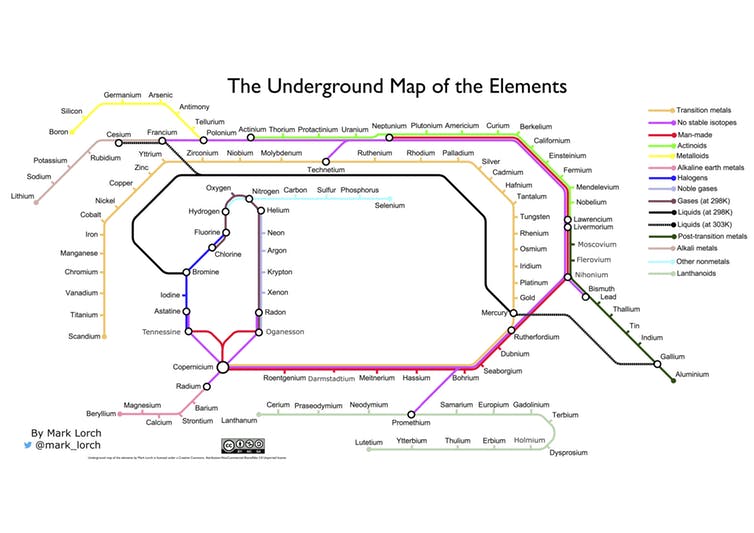
A tabela periódica poderia ter sido muito diferente
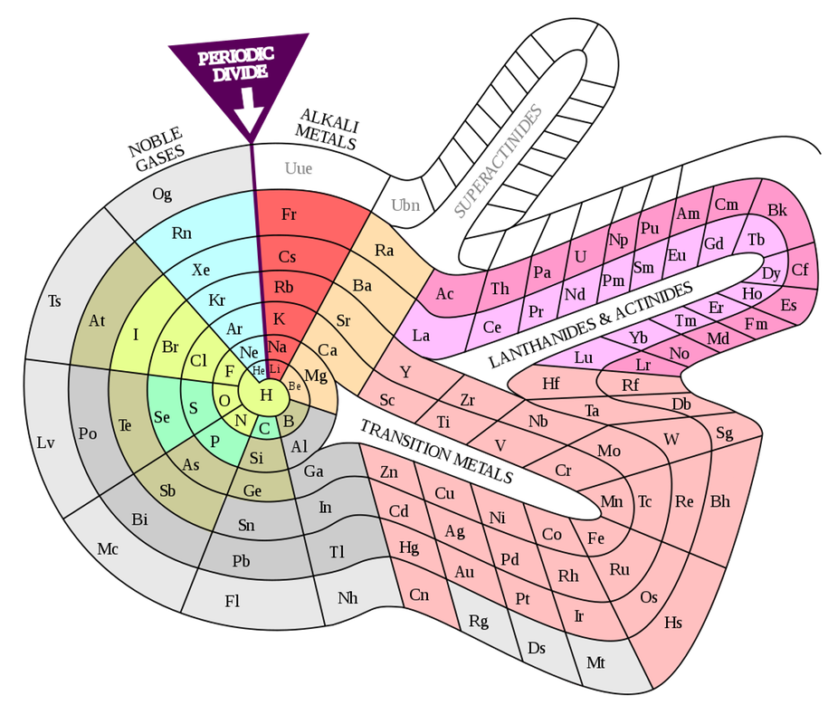
Versão espiral de Theodor Benfey (1964)
A famosa tabela periódica é onipresente nas escolas e nos laboratórios de química de todo o mundo.
O crédito para sua criação geralmente vai para Dimitri Mendeleev. Em 1869, o químico russo escreveu os elementos conhecidos – 63 na época – em cartões e os organizou em colunas e linhas de acordo com suas propriedades químicas e físicas.
Para celebrar o 150º aniversário deste momento crucial da ciência, a Organização das Nações Unidas proclamou 2019 como o “ano internacional da tabela periódica”.
As tentativas de classificação
Vale observar que Mendeleev não foi o primeiro a tentar classificar os elementos. Ao longo dos anos, muitos cientistas se propuseram a organizá-los de diferentes formas.
Décadas antes do russo, por exemplo, o químico John Dalton elaborou uma tabela, bem como alguns símbolos bastante interessantes para os elementos. Não pegou.
E, apenas alguns anos antes de Mendeleev, John Newlands também criou uma tabela classificando os elementos por suas propriedades.
O pulo do gato da versão de Mendeleev foi o que o cientista deixou de fora de sua classificação. Ele reconheceu que certos elementos estavam faltando, ainda a serem descobertos. Então, onde Dalton, Newlands e outros escreveram somente o que era conhecido, Mendeleev deixou espaço para o desconhecido. Ainda mais surpreendente, ele previu com precisão as propriedades dos elementos que faltavam.
A tabela de Mendeleev

Mendeleev deixou alguns pontos de interrogação em sua tabela. Por exemplo, ao lado de Al (alumínio) há espaço para um metal desconhecido. O químico previu que teria uma massa atômica de 68, uma densidade de seis gramas por centímetro cúbico e um ponto de fusão muito baixo.
Seis anos depois, Paul Émile Lecoq de Boisbaudran isolou o gálio com uma massa atômica de 69,7, uma densidade de 5,9g/cm³ e um ponto de fusão tão baixo que se torna líquido na mão.
Mendeleev fez o mesmo para o escândio, o germânio e o tecnécio (que só foi descoberto em 1937, 30 anos após sua morte).
Apesar disso, existem também diferenças fundamentais entre essa primeira versão de Mendeleev e a tabela com que estamos acostumados. Por um lado, a atual tem um monte de elementos que o russo ignorou e não deixou espaço para, principalmente os gases nobres (como hélio, néon e argônio). Além disso, a tabela inicial é orientada de maneira diferente que a versão moderna, com elementos que agora colocamos juntos em colunas dispostas em linhas.
A tabela atual
Quando damos um giro de 90 graus à tabela de Mendeleev, a semelhança com a versão moderna se torna aparente.
Por exemplo, os halogênios – flúor (F), cloro (Cl), bromo (Br) e iodo (I, com o símbolo J na tabela de Mendeleev) – todos aparecem próximos um do outro. Hoje, estão organizados na 17ª coluna da tabela (ou grupo 17).
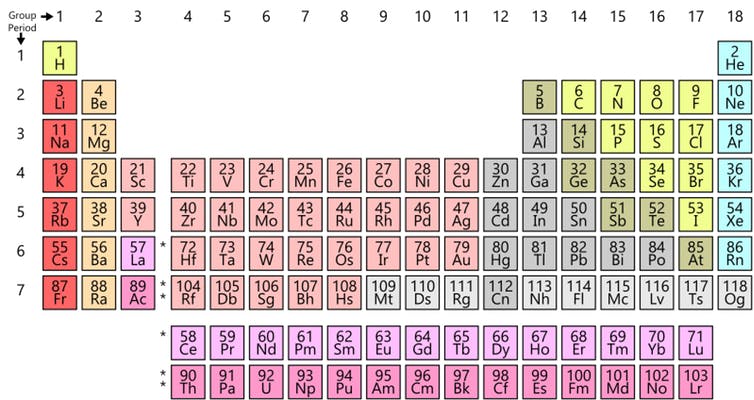
Tabela atual
O surgimento e a evolução da tabela de Mendeleev, no entanto, não significaram o fim da experimentação. Houveram muitas tentativas de dar layouts alternativos para os elementos.
Versões alterativas
Um exemplo particularmente notável é a espiral de Heinrich Baumhauer, publicada em 1870, com o hidrogênio no centro e elementos com massa atômica crescente girando para fora.
Os elementos que caem em cada um dos raios da roda compartilham propriedades comuns, assim como aqueles em uma coluna (ou grupo) na tabela de hoje:

Outra formulação estranha foi uma em formato de “infinito” de Henry Basset, criada em 1892:
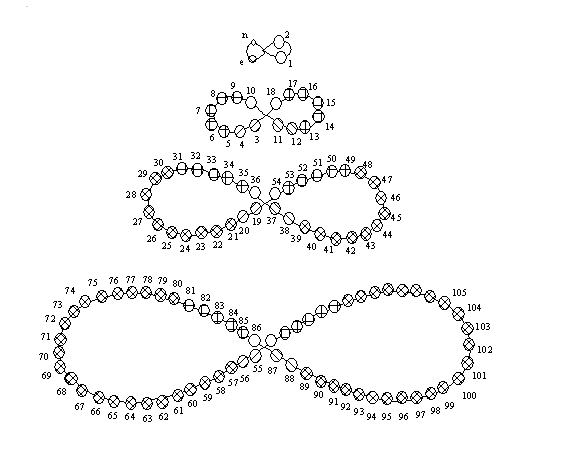
No início do século XX, a tabela se estabeleceu em um formato horizontal, como a versão aparentemente contemporânea de Alfred Werner em 1905:
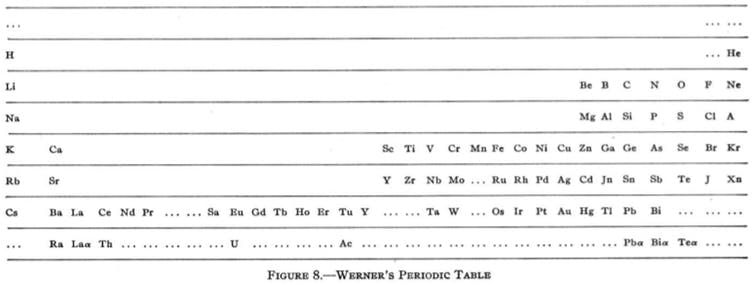
Pela primeira vez, os gases nobres apareceram em sua posição à direita da tabela. Werner também deixou lacunas para futuras descobertas, embora tenha exagerado nas suas previsões, com sugestões de elementos mais leves que o hidrogênio, bem como um entre o hidrogênio e o hélio (que não existem).
Uma versão particularmente influente foi a de Charles Janet, de 1928. Ele adotou a abordagem de um físico para a tabela, usando uma teoria quântica recém-descoberta para criar um layout baseado em configurações de elétrons. A tabela resultante é até hoje privilegiada por muitos físicos.
Curiosamente, Janet também forneceu espaço para elementos até o número 120, apesar de apenas 92 serem conhecidos na época. Estamos agora com 118:

A tabela atual é uma evolução direta da versão de Janet. O problema com o antigo formato é que ele é muito alongado e não cabe bem em uma página ou pôster. Portanto, em grande parte por razões estéticas, os elementos do bloco f são geralmente cortados e depositados abaixo da tabela principal. Foi assim que chegamos à versão reconhecida hoje.
Brincando com a tabela
Mostramos apenas algumas variações da tabela periódica neste artigo, mas existem literalmente centenas, muitas vezes desenhadas como uma tentativa de destacar correlações entre elementos que não são aparentes na tabela convencional.
Para conhecer algumas dessas variações, você pode conferir o banco de dados de Mark Leach (em inglês), com versões espirais, em 3D e muitas outras bizarras ou divertidas.
Como esta, criação do químico Mark Lorch, que funde dois gráficos icônicos, a tabela de Mendeleev e o mapa do metrô de Londres: [TheConversation]