Por que proteínas fluorescentes de águas-vivas revolucionaram a ciência

Proteínas fluorescentes mudaram a ciência. Pelo menos é isso que pensa o químico Marc Zimmer. Retiradas de águas-vivas brilhantes, estas proteínas são agora uma das ferramentas mais importantes da medicina, usadas para todo tipo de fins, desde o mapeamento do cérebro à pesquisa de doenças graves.
“Assim como a invenção do microscópio óptico abriu janelas para o mundo pequeno demais para ser visto a olho nu, as proteínas fluorescentes são usadas para iluminar proteínas de maneiras novas e maravilhosas, o que nos permite observar facetas inéditas de doenças”, explica Zimmer, autor do livro “Illuminating Disease” (algo como “Iluminando Doenças”, ainda sem edição em português).
A obra traz detalhes da história de parasitas e vírus fluorescentes geneticamente modificados, e como eles fornecem aos cientistas informações sobre a propagação de doenças como a malária, AIDS e dengue. Por exemplo, mosquitos geneticamente modificados com gônadas brilhantes podem ajudar a impedir a propagação da malária.
Abaixo, confira imagens que ilustram o livro do químico, com legendas fornecidas pelo próprio Zimmer sobre o que você está vendo neste mundo fluorescente.
Geleia-de-cristal

A água-viva geleia-de-cristal (Aequorea victoria, imagem acima) tem cerca de 300 foto-órgãos (imagem abaixo) na borda inferior do seu corpo em formato de guarda-chuva. Esses órgãos podem emitir luz verde e são a fonte original da proteína fluorescente verde (GFP, na sigla em inglês), utilizada em mais de 1 milhão de experiências por ano.
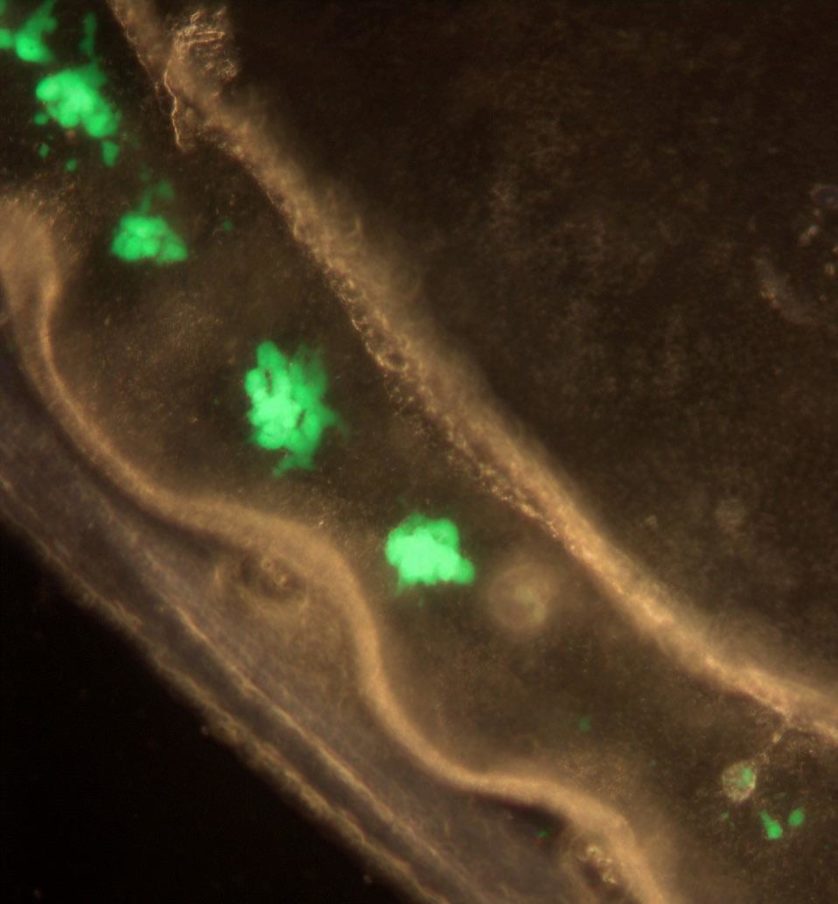
Malária
A imagem acima mostra parasitas da malária geneticamente modificados com GFP, para que suas glândulas salivares brilhem. Quando o mosquito pica a vítima, parasitas verdes entram na corrente sanguínea do hospedeiro e começam a corrida para seu fígado. Mesmo se as glândulas salivares de mosquitos contiverem mais de 20 mil parasitas, não mais do que mil são ejetados a cada vez.
Dengue
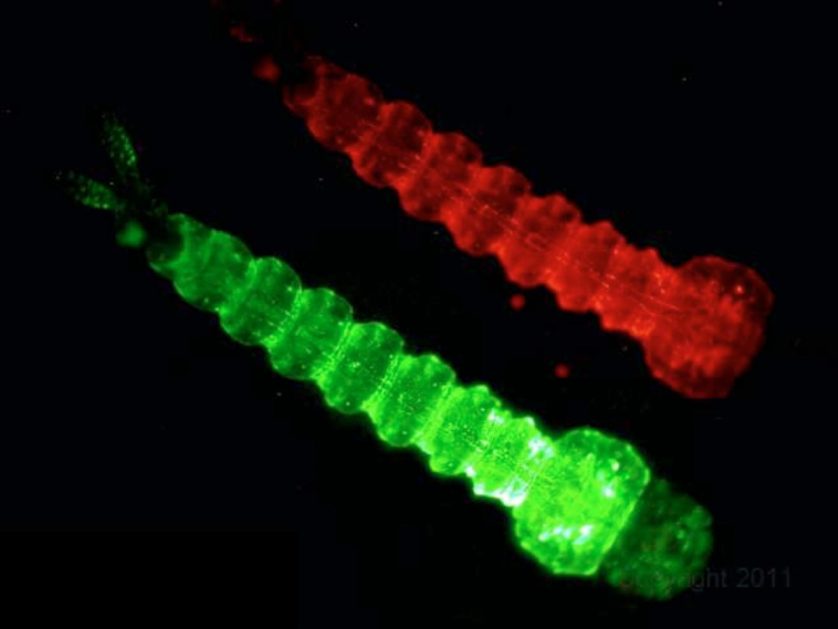
Mosquitos Aedes aegypti transmitem a dengue. Uma pequena empresa de biotecnologia, Oxitec, modificou geneticamente os insetos para que produzam filhotes que não passam da fase larval. Os mosquitos geneticamente modificados também contêm proteínas fluorescentes, de modo que podem ser distinguidos dos mosquitos selvagens. Esses insetos autodestrutivos contiveram com sucesso a propagação da dengue em partes do Brasil.
Gripe aviária

O pintinho à direita foi geneticamente modificado com GFP para diferenciá-lo de pintinhos normais. Ele tem uma sequência de RNA que impede a transmissão do vírus influenza A, da gripe aviária.
Arco-íris cerebral
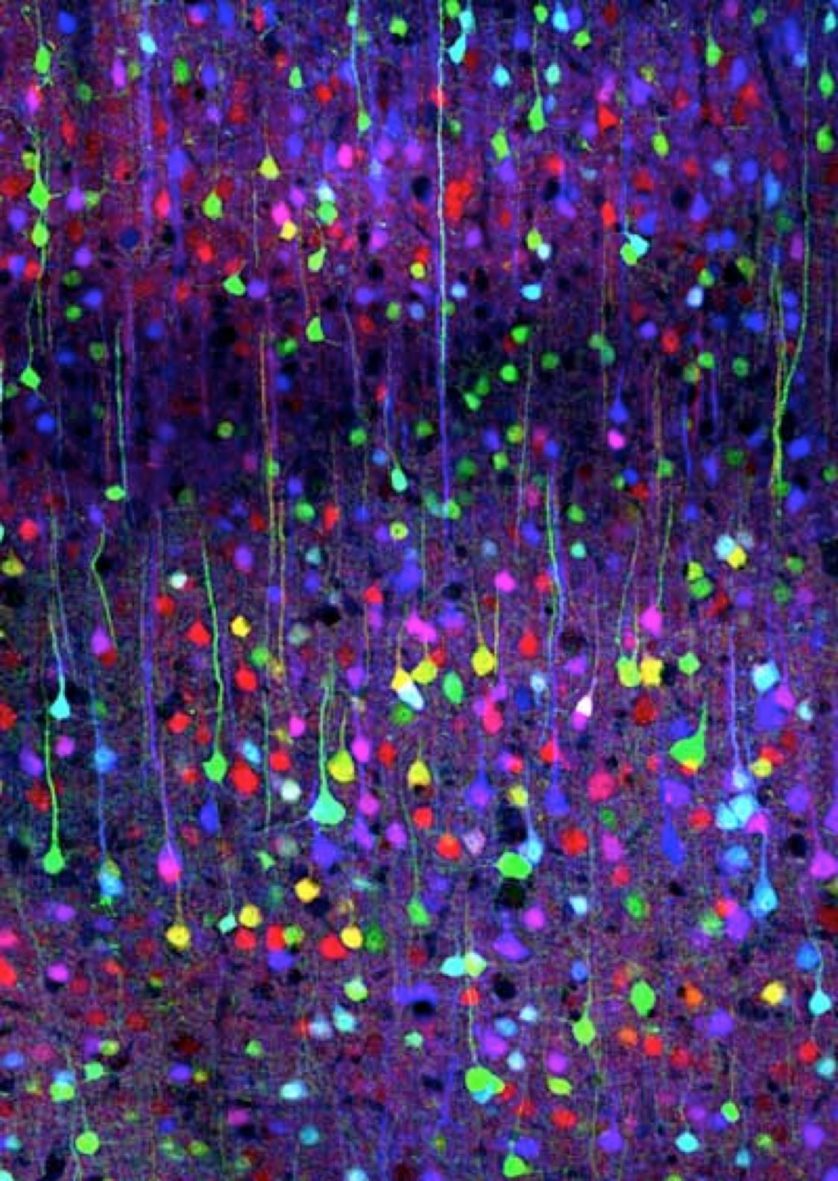
Todo um espectro de cores pode ser criado aleatoriamente pela mistura de proteínas fluorescentes vermelhas, verdes e azuis. A imagem acima mostra neurônios individuais no córtex cerebral de um rato, com cores diferentes. A técnica é chamada de “Brainbow” (uma mistura das palavras em inglês “brain”, para “cérebro”, e “rainbow”, para “arco-íris”).
Ataque cardíaco
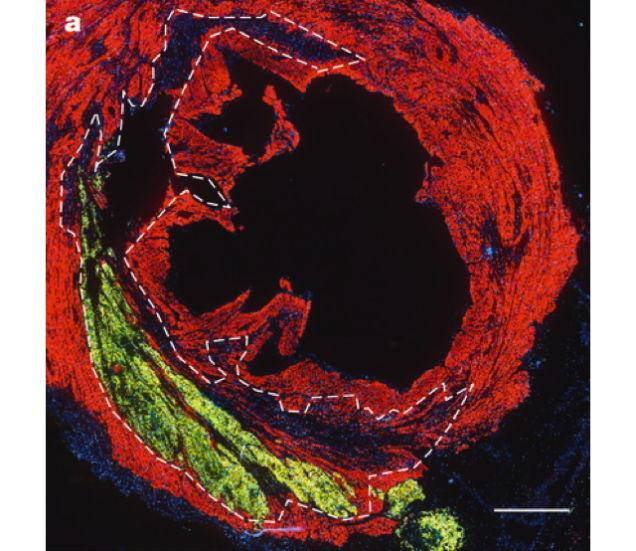
Essa é uma imagem microscópica confocal de um coração de macaco submetido a um ataque cardíaco e injetado com um bilhão de células-tronco humanas que expressam a proteína verde fluorescente GFP. As células-tronco humanas se diferenciaram e tornaram-se células musculares do coração verdes fluorescentes, incorporadas no coração do animal. A região delimitada dentro da linha pontilhada foi diretamente afetada pelo ataque cardíaco.
Gônadas brilhantes
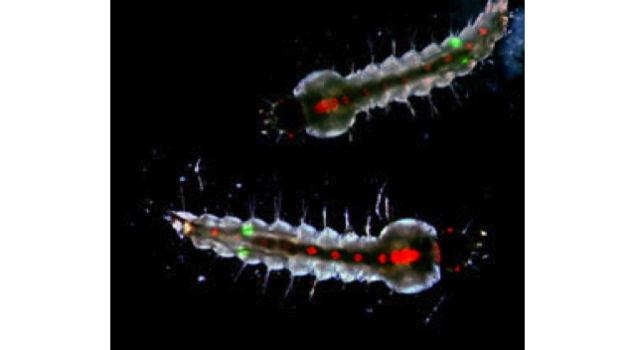
Essa foto mostra duas larvas do mosquito macho da malária. Seu gênero é facilmente determinado observando a presença de um par de testículos fluorescentes verdes.
As fêmeas desse inseto fazem sexo apenas uma vez na vida. Se a primeira e única vez que acasalarem o fizerem com um macho estéril, não produzem nenhuma prole. Isso pode controlar populações de pragas, uma abordagem chamada de “técnica do inseto estéril”, usada desde meados da década de 1950. Todos os anos, centenas de milhões de machos esterilizados são liberados na natureza. Eles podem ter relações sexuais mais de uma vez e passam a vida à procura de fêmeas disponíveis. Se um número suficiente de machos estéreis é liberado repetidamente, pode ajudar a colapsar a população local da praga.
Para utilizar esta técnica para o controle de mosquitos transmissores da malária, cientistas têm que ser capazes de diferenciar entre larvas machos e fêmeas, daí as gônadas brilhantes.
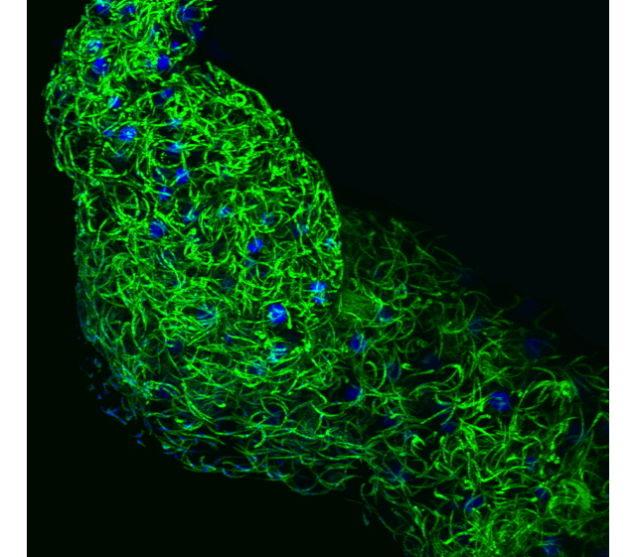
Verme
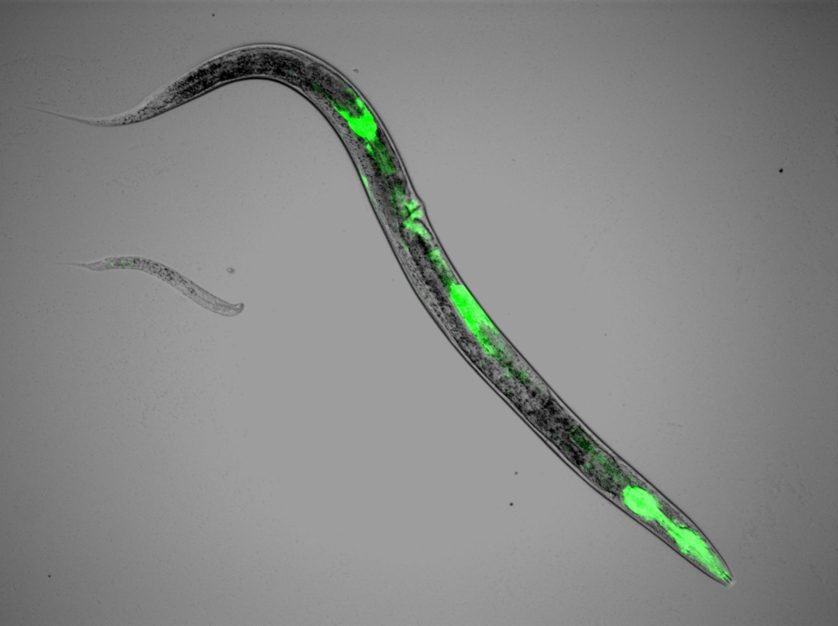
O verme C. elegans tornou-se um importante modelo para o estudo da biologia, especialmente do desenvolvimento, desde a década de 1970. A foto acima mostra um desses bichos geneticamente modificado com proteínas que cuidam do ritmo circadiano iluminadas por GFP.
A proteína é expressa na garganta, intestino e órgãos reprodutivos do verme. Quando a proteína ao redor do intestino é desativada, ele se torna constipado e só cresce a uma fração de seu tamanho normal (como o pequeno verme à esquerda). Sem a proteína do ritmo circadiano em sua garganta, não engole normalmente e se afoga em sua própria saliva. Já quando o gene na área reprodutiva é desligado, a vida sexual do verme se torna caótica. Os óvulos que atingem o esperma são ou muito jovens ou muito velhos para ser fecundados, e ele não tem praticamente nenhuma descendência. [Gizmodo]

